Introduction
Le cancer représente un problème majeur de santé publique en France. Le nombre de nouveaux cas de cancer est en effet estimé à 365 500 et le nombre de décès à 147 500 en 2011 (INCA 2011). Depuis 2004, le cancer est même devenu la principale cause de mortalité en France (AOUBA et alii 2011).
Grâce aux progrès de la science, 60% des cancers sont désormais curables. Mais de grandes disparités dans l'espérance de vie des patients persistent selon la localisation du cancer. Le cancer du sein a un taux de survie à 5 ans d'environ 85%, tandis que moins de 16% des hommes atteints d'un cancer du poumon sont en vie 5 ans après le diagnostic. Ce chiffre ne dépasse pas 5% pour le mésothéliome pleural (BOSSARD et alii 2007).
L'impact du cancer est très important aujourd'hui en raison de ces cancers qui sont encore difficiles à traiter. Si le cancer est considéré comme une maladie particulière, c'est aussi parce que nous ne guérissons jamais véritablement d’un cancer. Le traumatisme, les conséquences possibles et le risque constant de rechute ne nous permettent pas de considérer que la santé du patient est la même qu'avant la maladie. Le terme « guérison » est d’ailleurs généralement banni du vocabulaire du personnel soignant qui préfère le terme de «rémission».
Dans ce contexte, il est plus efficace de prévenir un cancer que de le soigner.
Les cancers professionnels sont généralement évitables en ce sens qu’en supprimant l’exposition au facteur de risque, on évite l’apparition de la maladie. La prévention des cancers professionnels représente donc un enjeu majeur en termes de santé publique, mais l'ampleur de ce problème est sous-estimée.
En France, la branche accidents du travail et maladies professionnelles de l'Assurance Maladie offre une indemnisation pour les maladies dont l’origine professionnelle est reconnue. Mais la sous-déclaration et la sous-reconnaissance des maladies professionnelles entraîne une invisibilité du nombre de cas de maladies professionnelles (GOLLAC et VOLKOFF 2006, THEBAUD-MONY 2006).
De plus, augmenter la santé et la sécurité sur un lieu de travail peut être perçu comme coûteux, la phase d’implantation d’un dispositif mobilisant des ressources. La crainte, pas toujours fondée, d’une éventuelle baisse des cadences de production liée aux mesures de prévention peut être un frein à la prévention dans les organisations. Le choix de la prévention est alors perçu par les entreprises, et parfois par le décideur public, comme un arbitrage entre santé des travailleurs et santé des entreprises.
L’économie de la santé a donc un rôle déterminant à jouer à la fois dans l’aide à l’allocation des ressources mais aussi dans l’incitation à la prévention. Une évaluation du coût social des cancers imputables à des facteurs de risque professionnels peut mettre en évidence les facteurs de risque dont l’impact économique est important pour la société.
L’objectif de ce papier est d’estimer le coût social des cancers professionnels en France. L'inhalation étant la principale voie de pénétration des substances cancérogènes (IMBERNON 2003) en milieu professionnel, nous avons choisi de restreindre notre analyse aux cancers des voies respiratoires. Nous incluons donc les cancers du larynx (CIM10: C32), du poumon (C33-34), les cancers nasosinusiens (C30-31) et les mésothéliomes de la plèvre (C45, C38.4).
Dans un premier temps, nous estimons, selon la méthode des risques attribuables, le nombre de cas (incidents, prévalents et de décès) de cancer du poumon, naso-sinusien, du larynx et de mésothéliome de la plèvre imputable à chaque facteur de risque pour l’année 2010 en France.
Nous mobilisons ensuite la méthode du coût de la maladie pour estimer les coûts que représentent ces cancers pour la société française selon l’approche par la prévalence. Nous estimons les coûts directs hospitaliers (séjours en médecine chirurgie obstétrique, radiothérapie privée, molécules onéreuses et missions d’intérêt général et d’aide à la contractualisation) et des soins de ville ainsi que les coûts indirects de morbidité (absentéisme et présentéisme) et de mortalité dans les sphères marchande et non marchande.
Méthode
La sélection des facteurs de risque
Pour surmonter la sous-reconnaissance des cancers professionnels en France, nous prenons en compte les facteurs de risque pour lesquels il existe un tableau des maladies professionnelles mais également ceux pour lesquels il n’en existe pas mais qui sont classés 1 ou 2A par le Centre international de recherche sur le cancer, c’est-à-dire cancérogène avéré ou probable. Nous aboutissons ainsi à une première liste de 45 facteurs de risque. Les facteurs pour lesquels aucune donnée n'est disponible, ainsi que ceux pour lesquels le nombre de personnes exposées est inférieur à 5000 ont été exclus. Après divers regroupements, nous retenons la liste suivante de 24 facteurs de risque des cancers professionnels des voies respiratoires :
Cancer du poumon
Acrylamide
Amiante
Arsenic (poussières et vapeurs)
Béryllium et composés
Brouillards d'acides minéraux forts contenant l'acide sulfurique (exposition professionnelle)
Cadmium et ses composés
Caoutchouc (industrie du)
Chrome VI et composés
Cobalt et carbure de tungstène (avant frittage)
Epichlorhydrine
Expositions professionnelles lors de l'épanage et de l'application d'insecticides non arsenicaux
Fumées d'échappement des moteurs diesels
Hydrocarbures Aromatiques Polycycliques
Nickel (grillage des mattes)
Nitrosamines en particulier n-nitrosodiméthylamine et n-nitrosodiéthylamine
Peintres (exposition professionnelle)
Rayonnements ionisants (par inhalation)
Silice cristalline
Tabagisme passif
Tétrachloréthylène (perchloréthylène)
Toluènes-α chlorés (benzotrichlorure, chlorure de benzal, chlorure de benzyle) et chlorure de benzolyne (expositions mixtes)
Verrerie d'art, fabrication de verre creux et de verre moulé
Cancer naso-sinusien
Chrome VI et composés
Epichlorhydrine
Poussières de bois
Poussières de cuir
Nickel (grillage des mattes)
Cancer du larynx
Amiante
Brouillards d'acides minéraux forts contenant l'acide sulfurique (exposition professionnelle)
Hydrocarbures Aromatiques Polycycliques
Mésothéliome de la plèvre
Amiante
La méthode des risques attribuables
Le calcul du risque attribuable est une méthode fréquemment utilisée en matière de santé publique pour estimer l'impact d'un facteur de risque sur la santé d'une population. On peut définir le risque attribuable de deux façons différentes. Il estime la fraction des cas d’une maladie attribuables à une exposition dans l’ensemble d’une population, y compris chez les individus non exposés (BOUYER et alii 1995). Autrement dit le risque attribuable évalue la fraction de cas qui pourrait être évitée si l’exposition était supprimée.
Formule de LEVIN (1953) :
Risque attribuable = (Pe × (RR-1)) / ([Pe × (RR-1) +1])
Avec Pe la prévalence d’exposition et RR le risque relatif.
Le risque attribuable s’exprime en proportion de cas qui peut aisément être transformé en nombre de cas (prévalents, incidents ou de décès) attribuable à l’exposition étudiée en appliquant la formule suivante :
Nombre de cas attribuables = RA x N
Avec RA le risque attribuable et N le nombre de cas (incidents, prévalents ou de décès) total de la pathologie dans la population concernée.
Risque relatif
Pour les données de risque relatif, nous avons mis en place une revue de littérature restreinte aux méta-analyses en interrogeant la base de données Medline sur PubMed. Le mésothéliome de la plèvre constitue un cas particulier dans notre analyse. Il est fréquemment appelé « cancer de l’amiante » puisque l’amiante est le seul facteur de risque reconnu du mésothéliome. De plus, le programme national de surveillance du mésothéliome permet de recueillir tous les cas incidents dans 21 départements français et d’estimer directement le risque attribuable à l’amiante (GOLDBERG et alii 2006). Pour cette pathologie, nous mobilisons donc directement les estimations de risque attribuable issues de ce programme. La revue de la littérature ne concerne donc pas le mésothéliome de la plèvre.
Pour l’ensemble des 24 facteurs de risque, la recherche a abouti à 393 résultats. L’épichlorydrine et l’acide sulfurique n’ont donné aucun résultat dans la base de données. La recherche pour l’acrylamide, le béryllium et les poussières de cuir n’a abouti qu’à une seule réponse et seulement deux pour les nitrosamines.
Tous les résultats de la recherche ne sont pas pertinents. Nous avons donc mis en place une série de critères pour sélectionner les études pertinentes. Dans un premier temps, toutes les études qui n’estiment pas un risque relatif à partir d’une méta-analyse ont été exclues. Ce critère permet d’éliminer les études qui ne sont pas des méta-analyses et celles qui n’estiment pas l’intensité d’une association entre un facteur de risque et une pathologie.
Trois critères d’exclusion davantage restrictifs sont ensuite appliqués successivement. Les résultats sont d’abord exclus si la population n’est pas adéquate. C’est le cas par exemple des études basées sur une population d’enfants. Pour les résultats dont la population est pertinente, la pathologie est étudiée. Seuls les résultats qui s’intéressent à un cancer des voies respiratoires (Poumon, larynx et naso-sinusien) sont retenus. En dernier lieu, nous vérifions si le facteur de risque est pertinent. Seuls les résultats correspondant à la liste des 24 facteurs de risque sont retenus. Dans le cas contraire, le résultat est exclu.
Les 393 résultats obtenus par la recherche Medline ont abouti à la sélection de 22 articles (cf annexe 1). Les seules estimations retenues pour l’intensité de l’association entre les poussières de cuir et le cancer naso-sinusien sont 2,71 pour les femmes et 1,92 pour les hommes. Pour les autres facteurs de risque, une fourchette d’estimation de risque relatif est retenue selon le genre.
Prévalence d'exposition
La prévalence d’exposition est la proportion d’individus exposés à un facteur de risque au sein d’une population. On distingue la prévalence « instantanée » qui s’intéresse à une exposition à un moment donné et la prévalence « vie entière » qui estime le pourcentage de personnes ayant été exposées au facteur de risque au moins une fois dans leur vie professionnelle. En ce qui concerne l’étude des risques dans le domaine de la santé, la prévalence d’exposition « vie entière » est plus adaptée. Elle permet de tenir compte à la fois du temps de latence entre l’exposition à un facteur et l’apparition du cancer mais aussi des changements d’emploi des individus au cours de leur vie professionnelle.
Le programme Matgéné développe une matrice emplois-expositions « multi nuisances » spécifiquement adaptée à la population générale française. Il permet d’étudier l’exposition de la population française à des nuisances chimiques tout au long de la vie professionnelle (ARSLAN et alii 2006).
Les prévalences d’exposition « vie entière » issues du programme Matgéné sont donc privilégiées. Lorsque les données ne sont pas disponibles, nous mobilisons les données de l’enquête Sumer. Ces données correspondent à une exposition à un moment donné. Pour estimer les valeurs « vie entière », les données peuvent être multipliées par 3 (AUTIER et alii 2007) ou 4 (NELSON et alii 2005, STEENLAND et alii 2003). Ce facteur représente le nombre moyen de changement de poste durant une carrière professionnelle. Pour notre analyse, nous multiplions les données de prévalence d’exposition « instantanée » par un facteur 3.
Aucune source ne fournit de données d’exposition pour les peintres. Dans ce cas particulier, nous considérons les individus appartenant à la catégorie socioprofessionnelle « peintres et ouvriers qualifiés de pose de revêtements sur supports verticaux » comme exposés.
Il n’existe pas de données de prévalence d’exposition Matgéné et Sumer pour le tabagisme passif, les hydrocarbures aromatiques polycycliques et l’industrie du caoutchouc. Ces facteurs de risque ne sont pas pris en compte dans notre analyse qui inclut donc l’amiante, le chrome, la silice cristalline, les fumées d’échappement des moteurs diesel, les peintres, les poussières de bois et les poussières de cuir.
Morbidité et mortalité
Les données en termes de nombre de cas de cancer (incident, prévalent et de décès) pour l’année 2010 sont issues de la littérature ou sont extrapolées à partir des données disponibles pour les années précédentes.
Les calculs effectués nous permettent d’estimer pour l’année 2010 l’incidence du mésothéliome de la plèvre à 893 nouveaux cas. L’incidence du cancer naso-sinusien est évaluée à 510 cas pour les hommes et 247 cas pour les femmes.
Pour cette même année, les nombres de cas prévalents de cancer du poumon et de mésothéliome de la plèvre sont estimés respectivement à 35 990 et 652 cas pour les hommes contre 8 852 et 244 cas pour les femmes. Selon nos estimations, le cancer du larynx représente 11 806 cas prévalents pour les hommes et 1 318 cas prévalents pour les femmes pour l'année 2010.
Le nombre de décès par cancer naso-sinusien est évalué à 138 pour les hommes et 60 pour les femmes. Pour le mésothéliome de la plèvre, l’estimation des décès est de 572 pour les hommes et 238 pour les femmes.
L’évaluation des coûts
Nous avons estimé le nombre de cas de cancers imputables à chacun des facteurs de risque. Nous évaluons à présent le coût que représentent ces cancers pour la société. Pour cela, des équations ont été créées pour chaque catégorie de coût. Nous développons ici uniquement la méthodologie générale, les équations sont disponibles dans le détail en annexe 2.
Les coûts directs
Pour estimer le coût direct des cancers du poumon, du larynx, des naso-sinus et des mésothéliomes de la plèvre imputables aux facteurs de risque étudiés, nous estimons dans un premier temps un coût direct annuel moyen que nous multiplions ensuite par le nombre de cas de chaque cancer imputables aux facteurs de risque.
Pour estimer le coût direct annuel moyen des cancers pour l’année 2010, nous partons de l’étude menée par AMALRIC (2007) qui est elle-même basée sur le travail pionnier de BORELLA et alii (2000 et 2002).
Les auteurs ont crée un algorithme permettant d’extraire de la base nationale des résumés de sortie anonyme les séjours relatifs à un cancer. Ces séjours sont ensuite valorisés à l’aide de l’étude nationale des coûts (ENC). AMALRIC (2007) actualise ces données pour l’année 2004 et prend également en compte les coûts de la radiothérapie privée, des molécules onéreuses, des missions d’intérêt général et d’aide à la contractualisation (MIGAC) et des soins de ville qui ne sont pas pris en compte dans le programme de médicalisation des systèmes d’information (PMSI).
Les données sont disponibles par grande localisation, c’est-à-dire pour les cancers des voies aérodigestives supérieures (VADS) et de l’appareil respiratoire. Nous estimons tout d’abord le coût direct de l’ensemble des cancers des VADS et de l’appareil respiratoire pour l’année 2010.
Séjour en MCO et radiothérapie privée
Pour évaluer les coûts des séjours en médecine chirurgie obstétrique (MCO) et de la radiothérapie privée pour l’année 2010, nous actualisons les estimations de 2004 issues de l’étude d’Amalric en tenant compte de l’évolution du coût moyen des groupes homogènes de malades correspondants à partir de l’ENC.
Molécules onéreuses et MIGAC
Les MIGAC permettent de financer des missions d’intérêt général de l’hôpital public. Les MIGAC inclut notamment les missions d’enseignement, de recherche, de référence et d’innovation (MERRI). La question de l’inclusion des coûts de la recherche dans les évaluations de type COI fait débat. Nous incluons les coûts de l’ensemble des MIGAC relatif aux cancers à l’exception des MERRI qui correspondent au financement de la recherche. AMALRIC (2007) estime la part des enveloppes MIGAC et MERRI relative aux cancers respectivement à 10,5% et 26%. A partir des données de 2010, nous estimons le montant des MIGAC (hors MERRI) relatifs à l’ensemble des cancers.
Les dépenses pour les molécules onéreuses sont disponibles pour l’ensemble des cancers pour l’année 2010.
Pour les molécules onéreuses et les MIGAC cancer, nous répartissons les données pour 2010 selon les grandes localisations en utilisant les clés de répartition issues de l’étude d’Amalric.
Soins de ville
Le coût des soins de ville est estimé directement à partir du coût direct hospitalier. Il représente 29% du coût direct total pour les cancers des voies respiratoires et 32% pour les cancers des VADS.
Il est possible d’approximer le coût moyen des cancers en divisant le coût de la prise en charge pour une localisation par l’incidence correspondante (BORELLA et PARAPONARIS 2002). Nous reprenons cette méthodologie pour estimer un coût moyen par cas et par localisation. Nous faisons l’hypothèse que le coût direct moyen des cancers du poumon et des mésothéliomes de la plèvre est égal au coût direct moyen des cancers de l’appareil respiratoire et que le coût moyen des cancers naso-sinusiens et du larynx est identique au coût moyen des cancers des VADS.
Les coûts indirects
Nous avons élaboré une typologie des coûts à partir de laquelle nous définissons les coûts indirects comme les pertes de production marchandes et non marchandes, liées à une diminution ou une absence de productivité causées par le décès ou l’état de santé de l’individu. Nous distinguerons donc les coûts de morbidité (absentéisme et présentéisme) et les coûts de mortalité dans les sphères marchandes et non marchandes.
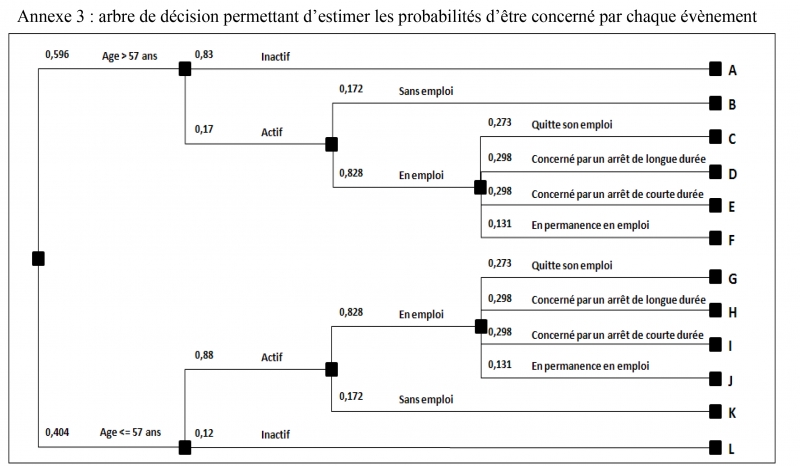
Pour prendre en compte toutes ces catégories de coûts indirects, sans risque de double compte, nous avons créé un arbre de décision pour estimer la probabilité d'être concerné par chaque catégorie de coûts. Nous incluons ce paramètre dans nos modèles d'évaluation des coûts indirects.
Pour développer l'arbre de décision, nous mobilisons des données de taux d'activité et de taux d'emploi spécifiques des patients atteints d'un cancer, mais également des données sur l'impact du cancer sur leur vie professionnelle (cf annexe 3).
Parmi ceux qui sont employés, MALAVOLTI et alii (2006) fournissent des estimations sur le pourcentage d’entre eux qui deux ans après le diagnostic a perdu ou quitté son emploi ; a repris son activité ; n’a jamais interrompu son activité ; est resté en permanence en emploi ; n’a encore jamais repris son activité. Nous considérons que les individus qui n’ont jamais repris leur activité au bout de deux ans correspondent à la population de personnes affectées par des absences de longue durée. Nous supposons que ceux qui ont repris leur activité sont affectés par des absences de courte durée. Nous faisons également l’hypothèse que les statistiques sur la situation professionnelle sont applicables à l’année.
Les coûts indirects de morbidité
Les coûts de la morbidité incluent les coûts liés à des absences au travail de courte ou de longue durée, les coûts liés au présentéisme ainsi que les pertes de production dans la sphère non marchande.
Les coûts d'absentéisme sont évalués à la fois par la méthode des coûts de friction et la méthode du capital humain. Pour estimer la valeur annuelle des pertes de production selon la méthode du capital humain, nous multiplions le nombre moyen de jours d’arrêts de travail par an par la valeur quotidienne des pertes de production que nous estimons en divisant la part du produit intérieur brut relative à la rémunération des salariés par la population active. Selon la méthode des coûts de friction, la production de l'employé absent n'est pas totalement perdue. Nous avons retenu l'hypothèse couramment utilisés d'une perte de seulement 80% de la production (KOOPMANSCHAP et alii 1995).
Le présentéisme est défini comme la réduction de productivité imputable à une maladie pour les personnes qui continuent de travailler (SCHULTZ et EDINGTON 2007).
GOETZEL et alii (2004) estiment la baisse de productivité annuelle imputable à un cancer à 8,5 %.
Les coûts indirects de morbidité dans la sphère non marchande correspondent aux pertes d’activités domestiques causées par le cancer. Nous prenons en compte ces coûts uniquement pour les personnes sans emploi.
Nous estimons les pertes de production dans la sphère non marchande selon la méthode du coût de remplacement et nous valorisons chaque heure consacrée à une tâche domestique par le salaire horaire minimum correspondant à 8,86 euros.
Les données sur le nombre d'heures de tâches domestiques effectuées par les individus sont issues de l'étude de ROY et alii (2011). Nous ne conservons pas la définition la plus restrictive des tâches domestiques puisque ces activités sont toujours réalisées quel que soit le temps disponible. Nous utilisons la définition médiane et nous prenons en compte seulement les activités réalisées pour leur propre foyer. Le temps consacré aux tâches domestiques par jour est estimé à 3 heures et 17 minutes. Chaque individu consacre une moyenne de 1197,2 heures par an pour les activités domestiques.
Les coûts de mortalité
Pour estimer les coûts de mortalité, il faut tout d’abord estimer le nombre d’années de vie perdues puis les valoriser.
Pour évaluer les coûts de mortalité dans la sphère marchande, nous nous intéressons aux années de travail perdues. Nous faisons donc la différence entre l'âge moyen de départ à la retraite correspondant à 61,62 ans (CNAV 2011) et le centre de la tranche d'âge de l’individu au moment du décès.
Pour estimer les coûts indirects liés à la mortalité dans la sphère non marchande, il faut considérer deux situations distinctes. Soit l’individu n’était pas en emploi au moment du décès, les pertes de production qui en découlent touchent alors exclusivement la sphère non marchande et sont mesurées de l’âge du décès jusqu’à l’espérance de vie. Soit l’individu était en emploi et dans ce cas les pertes de production non marchandes correspondent aux années de vie perdues de l’âge de départ à la retraite jusqu’à l’espérance de vie. Nous supposons donc que tout individu, s’il n’était pas mort d’un cancer, n’aurait pas vécu plus longtemps que l’espérance de vie qui était de 78,1 ans pour les hommes contre 84,8 ans pour les femmes en 2010.
Résultats
En unités physiques
Les estimations de prévalence d’exposition « vie entière » sont utilisées avec les estimations de risque relatif issues de la revue de la littérature pour calculer les risques attribuables à chaque facteur de risque.
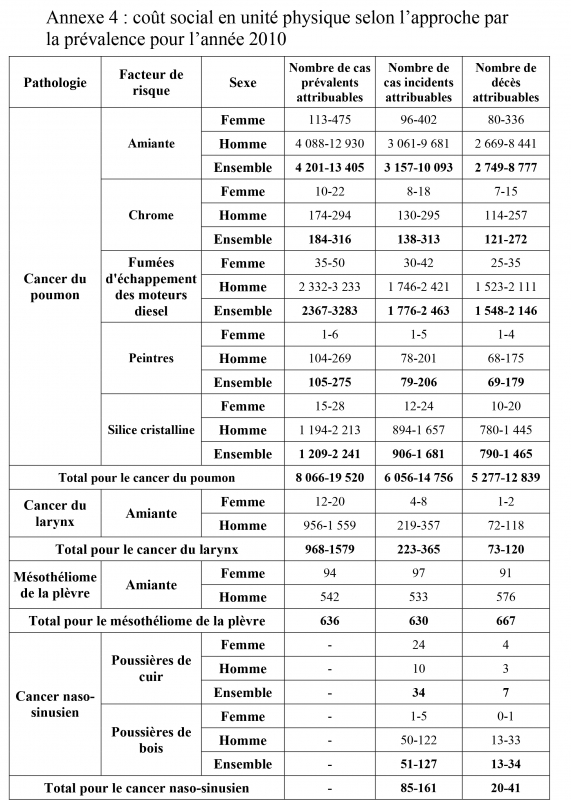
L’application des estimations de risques attribuables aux données de morbidité et mortalité des cancers nous permet d’estimer les nombres de cas incidents, de cas prévalents et de décès imputables à chaque facteur de risque pour l’année 2010 (cf annexe 4).
Nous estimons le nombre de cas incidents de cancer du poumon imputable à une exposition à l'amiante entre 3 157 et 10 093 pour l'année 2010. Selon nos calculs, l'exposition aux fumées d'échappement des moteurs diesel aurait causé entre 1 548 et 2 146 décès pour cette même année.
En unités monétaires
Les résultats sont présentés en annexe 5 par facteur de risque et par type de cancer. La valeur basse correspond à l'estimation basse du nombre de cas prévalents ou de décès et à l'utilisation de la méthode des coûts de friction pour évaluer les coûts indirects d'absentéisme. La valeur haute est basée sur l'estimation haute du nombre de cas prévalents ou de décès et l'utilisation de l'approche du capital humain.
Selon l'approche par la prévalence, le coût social des cancers du poumon, des cancers du larynx, des cancers naso-sinusiens et des mésothéliomes de la plèvre attribuables à l'amiante, au chrome, aux fumées d'échappement des moteurs diesel, aux peintres, à la silice cristalline, aux poussières de bois et de cuir en France est estimé entre 917 et 2 181 millions d'euros pour l'année 2010 dont 795 à 2 011 millions d'euros uniquement pour les facteurs de risque du cancer du poumon. Pour l’année 2010, le coût social des cancers du poumon imputables à une exposition à l’amiante est estimé entre 415 et 1 380 millions d’euros. Les fumées d’échappement des moteurs diesel et la silice cristalline représentent respectivement un coût pour la société estimé entre 233 et 336 millions d’euros et entre 119 et 229 millions d’euros.
Discussion
Nos estimations de cancers naso-sinusiens attribuables à l'exposition aux poussières de bois sont basées sur les données de risque relatif variant entre 1,17 (MANNETJE et alii 1999) et 3,9 (DEMERS et alii 1995). Ces estimations de risque relatif ont été calculées à partir d’études multicentriques et ne prennent pas en compte la spécificité du contexte français dans lequel l'utilisation de bois dur est plus fréquente en particulier dans la fabrication de meubles. Ainsi, dans une étude réalisée par IMBERNON (2003) un risque relatif de 10 est choisi comme scénario bas pour estimer le risque de cancer naso-sinusien imputable à une exposition aux poussières de bois en France. Notre évaluation ne prend pas en compte cette spécificité, le risque de cancers naso-sinusiens attribuables aux poussières de bois est sans doute largement sous-estimé.
Seulement 7 des 24 facteurs de risque identifiés ont abouti à l’estimation d’un coût social. Pour inclure davantage de facteurs de risque, il faut envisager de mener une revue de la littérature des risques relatifs non restreinte aux méta-analyses (qui inclurait les études cas-témoin et de cohortes notamment) et éventuellement de mettre en place des méta-analyses à partir des articles retenus.
Pour estimer le risque attribuable pour les peintres, nous avons considéré les individus appartenant aux groupes socio-économiques « peintres et ouvriers qualifiés de pose de revêtements sur supports verticaux », comme exposé. La prévalence exposition est probablement largement sous-estimée, puisque d'une part, tous les peintres n’appartiennent pas à cette catégorie professionnelle et d'autre part, la peinture peut être considérée comme une externalité négative et n'affecte pas seulement les peintres mais toutes les personnes présentes sur le chantier. Notre évaluation sous-estime donc le risque de cancer du poumon attribuable pour les peintres.
Conclusion
En conclusion, les principaux apports de ce travail se situent aussi bien dans la méthodologie développée que dans les résultats obtenus. La méthode a en effet été repensée pour permettre une prise en compte exhaustive des coûts indirects. Elle a également été adaptée au contexte des cancers professionnels. La combinaison d’une sélection des facteurs de risque et de la méthode des risques attribuables a permis de surmonter l’invisibilité de ces maladies professionnelles en France. L’évaluation fournit ainsi des estimations originales et récentes de coûts à la fois en unités physiques et monétaires, qui sont détaillées selon le sexe, le facteur de risque, la pathologie ou encore le type de coût.